何謂實證醫學
所謂實證醫學(Evidence-Based Medicine, EBM),又稱循證醫學,是一種從龐大的醫學資料庫中,以統計學與流行病學的方法,將資料進行分析而得出結論,並依此檢驗的結果制定出最佳的醫療決策的一種方式。而要得出令人值得信賴的醫療決策,其步驟包含從醫學資料庫中過濾出有意義值得信賴的資料,經嚴格評讀,綜合分析,再將所獲得的結論與臨床經驗及對病患最佳價值做整合。
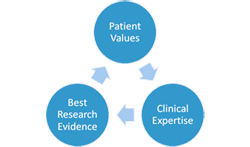 過去許多知識及文獻資料的取得只能從書本及專業雜誌,龐大資料查詢十分麻煩且費時。而現在許多知識及文獻資料可透過電腦網路與電子資料庫取得,醫師可以快速獲得大量醫療文獻及資料,並將所獲得的結論應用在日常醫療業務上。1990年代起隨著電腦網路發達,新興網路醫療資訊與傳統統計學及流行病學的結合進而催生了實證醫學的發展。藉由實證醫學的方法,將臨床所面臨的困難形成探討的題目,從龐大醫學資料查詢經過嚴格而系統性的評估,轉化成可行的醫療決策以解決臨床問題,並進一步檢討其成效,並形成新問題,再重複前述之步驟,其最終目的即是達到醫療人員不斷自我終身學習,並應用於臨床進而獲得最佳的醫療成效。
過去許多知識及文獻資料的取得只能從書本及專業雜誌,龐大資料查詢十分麻煩且費時。而現在許多知識及文獻資料可透過電腦網路與電子資料庫取得,醫師可以快速獲得大量醫療文獻及資料,並將所獲得的結論應用在日常醫療業務上。1990年代起隨著電腦網路發達,新興網路醫療資訊與傳統統計學及流行病學的結合進而催生了實證醫學的發展。藉由實證醫學的方法,將臨床所面臨的困難形成探討的題目,從龐大醫學資料查詢經過嚴格而系統性的評估,轉化成可行的醫療決策以解決臨床問題,並進一步檢討其成效,並形成新問題,再重複前述之步驟,其最終目的即是達到醫療人員不斷自我終身學習,並應用於臨床進而獲得最佳的醫療成效。
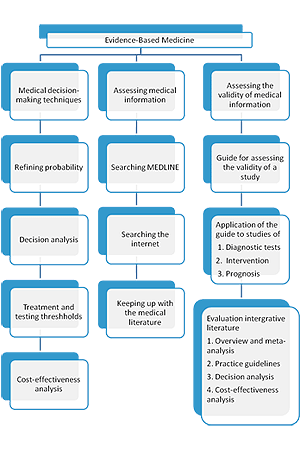 實證醫學是以病人為中心(patient-centered)、以其醫療問題為導向(problem-based),結合醫師個人的臨床經驗及最新的臨床研究結果來對任一病人做出最合理的診斷和治療之一種模式。目前最廣被接受的定義是根據英國牛津大學大衛.薩克特(David Sackett)教授所提:?各醫學相關領域專家以其良知,明確明智地應用世上現有衛生照顧領域中所可獲得的最佳證據文獻,解決個別病患的臨床問題?。其主要包含三大範疇:醫療決策技能(medical decision-making techniques),醫療資訊擷取(assessing medical information),醫療資訊效度之評估(assessing the validity of medical information)。
實證醫學是以病人為中心(patient-centered)、以其醫療問題為導向(problem-based),結合醫師個人的臨床經驗及最新的臨床研究結果來對任一病人做出最合理的診斷和治療之一種模式。目前最廣被接受的定義是根據英國牛津大學大衛.薩克特(David Sackett)教授所提:?各醫學相關領域專家以其良知,明確明智地應用世上現有衛生照顧領域中所可獲得的最佳證據文獻,解決個別病患的臨床問題?。其主要包含三大範疇:醫療決策技能(medical decision-making techniques),醫療資訊擷取(assessing medical information),醫療資訊效度之評估(assessing the validity of medical information)。
實證醫學三大範疇,摘錄自Daniel J.Friendland, Alan S.Go, J. Ben Davoren, Evidence-Based Medicine a Framework for Clinical Practice, 1998.
實證醫學發展史
1972年英國臨床流行病學者Archi Cochrane首先提出實證醫學的概念。他認為所有的醫療行為都必須根據經嚴謹研究後證實有效的數據,才能將醫療資源做最佳的應用進而達到對病人最好的治療結果。Cochrane認為衡量一個醫療行為是否有效,應該透過隨機對照臨床試驗(Randomized Controlled Trials, RCT)的方式。同時指出醫療資源應運用於經嚴謹研究證實有效的治療方向,才能提供合理的醫療服務。他並認為若沒有經常將相關醫療資訊進行整合分析,對醫療專業來說是一個非常嚴重的問題。而解決的方法就是各專科醫療人員應定期評讀摘錄及整合所有相關隨機對照臨床試驗之結果。
實證醫學(Evidence-Based Medicine, EBM)詞彙之源頭是1980年代由加拿大Mc Master大學發展臨床學習策略時所提出。當時腎臟科醫師David L. Sackett於加拿大Mc Master大學成立臨床流行病與統計學科為實證醫學教育推展的源頭。其目的即是推展醫療人員個人終身學習,利用將搜尋資料作有系統的評估整合,作為解決臨床醫療問題之方法。1984年John Wennberg提出即使治療同一種疾病的病人族群時,個體間還是會存在著無解釋的差異性。而這些差異往往造成醫療人員治療時的困惑,須將這些同一種疾病治療的差異性作廣泛性且系統性的評估及整合才能為這些困惑提出解答。1986年美國國會推動?病患成果評估研究計畫?,並於1989年成立?醫療照護政策和研究機構(Agency for Health Care Policy abd Research, AHCPR)?以指導醫療研究並公布研究結果及醫療作業準則。
實證醫學中心從1992年英國國家衛生服務院National Health Service Research and Development Program為紀念Archie Cochrane的貢獻,在牛津大學成立Cochrane Collaboration研究組織,希望與全世界專家針對各個醫學領域之隨機對照試驗作系統性評論,目前有英國、法國、美國、加拿大、澳洲、中國、巴西、荷蘭、義大利、西班牙、德國、挪威、南非等國家共15個Cochrane中心成立,並積極推動相關工作。希望能利用嚴謹且系統性的評估方法,從龐大的醫學研究資料庫中整理出截至目前為止各種醫療行為之結論性療效以改進醫療品質及資源運用。 Cochrane Collaboration 國際共同研究組織遵循Cochrane所提出對醫療行為之研究須合乎Randomized Controlled Trials的要求,系統性地隨時更新並發布醫療研究評讀的結果。
實證醫學的步驟
實行實證醫學有五個步驟﹝Five steps to practice EBM﹞包括:
- 第一步:形成一個可回答的臨床問題 ﹝Asking an answerable question﹞
- 第二步:搜尋最佳文獻證據﹝Tracking down the best evidence﹞
- 第三步:嚴格評讀文獻證據﹝Critical appraisal﹞
- 第四步:證據結論與臨床專業及病人價值結合及應用﹝Integrating the appraisal with clinical expertise and patients’preference﹞
- 第五步:評估執行效果及效用﹝Evaluation the effectiveness and efficiency in executing steps 1-4﹞
形成一個可回答的臨床問題﹝Asking an answerable question﹞
臨床問題的種類可分為:「背景問題」;Background question,及「前景問題」;Foreground question。所謂「背景問題」是對疾病某一個面向所提的問題或是對疾病基本認識不足所提出的問題,最常見的問題有六類:Who, What, Where, When, How, Why。例如(Who)誰比較會得糖尿病? (What)什麼是糖尿病? (Where)哪個地方的人比較會得糖尿病? (When)什麼年紀比較會得糖尿病? (How)糖尿病是如何形成的? (Why)為何會得糖尿病?「背景問題」的答案通常是對疾病基本知識,較不具爭議。對疾病有較深入的認識後才有辦法提出較深入的「前景問題」。
「前景問題」是比較深入性針對特定病患疾病之醫療處置的問題。通常有個重要元素才能形成一個較深入且精準的「前景問題」。包括:病患 Patient and/or Problem (P),處置Intervention (I),對照Comparison (C),臨床結果Outcome (O),可簡化為PICO模式。例如一位懷疑有壞死性筋膜炎的男性,我們欲了解使用X-ray或是使用MRI何者較能提高診斷的正確性?則P為一位懷疑有壞死性筋膜炎的男性,I為使用X-ray檢查,C為使用MRI檢查,O為何者較診斷正確性較高?提出一個可回答的「前景問題」是實證醫學的第一步。
搜尋最佳文獻證據﹝Tracking down the best evidence﹞
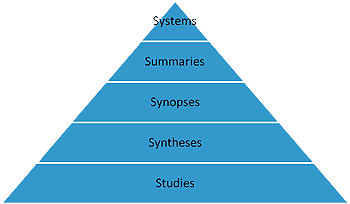 目前搜尋最佳實證資料庫有兩大類:一是使用原始文獻資料庫(primary journals or databases)如Medline或是Pubmed,二是直接使用經過整理的實證醫學資料庫(secondary journals or databases)。實證醫學文獻資料庫與一般原始醫學文獻資料庫最大的差異在於實證醫學文獻資料庫為評論性的文章,著重實際臨床的運用與研究,其文章質精但量少。而一般原始醫學文獻資料庫文章類型不一,量雖多但品質不定。實 證醫學資料庫(Evidence-Based Medicine, EBM resources)可以幫助醫療人員利用嚴謹的檢索策略收集重要的相關文獻,並有專家團隊嚴格評讀文獻證據並提供簡明扼要的建議或結論。可幫助醫療人員在短時間內從茫茫文獻大海中搜尋到需要且具結論性的文獻資料以解決臨床上的問題。到建議先直接使用經過整理的實證醫學資料庫﹝如CDSR, CCTR, DARE, ACP journal club﹞,萬一這些都找不到,可以從Medline等資料庫中搜尋。盡量搜尋與病人問題相同且證據等級(level of evidence)較高的文獻,再謹慎的評讀與評估其在此病人問題的適用性。
目前搜尋最佳實證資料庫有兩大類:一是使用原始文獻資料庫(primary journals or databases)如Medline或是Pubmed,二是直接使用經過整理的實證醫學資料庫(secondary journals or databases)。實證醫學文獻資料庫與一般原始醫學文獻資料庫最大的差異在於實證醫學文獻資料庫為評論性的文章,著重實際臨床的運用與研究,其文章質精但量少。而一般原始醫學文獻資料庫文章類型不一,量雖多但品質不定。實 證醫學資料庫(Evidence-Based Medicine, EBM resources)可以幫助醫療人員利用嚴謹的檢索策略收集重要的相關文獻,並有專家團隊嚴格評讀文獻證據並提供簡明扼要的建議或結論。可幫助醫療人員在短時間內從茫茫文獻大海中搜尋到需要且具結論性的文獻資料以解決臨床上的問題。到建議先直接使用經過整理的實證醫學資料庫﹝如CDSR, CCTR, DARE, ACP journal club﹞,萬一這些都找不到,可以從Medline等資料庫中搜尋。盡量搜尋與病人問題相同且證據等級(level of evidence)較高的文獻,再謹慎的評讀與評估其在此病人問題的適用性。
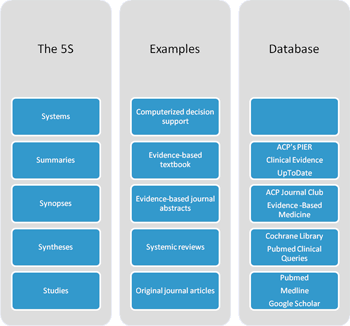 在實證醫學的觀念裡,文章是有等級的,亦即systematic review和meta-analysis的文章最有價值,single randomized controlled trial次之,其他類型的文章又次之,我們在搜尋文獻時也運用這個的觀念,先由重要的文章看起。
在實證醫學的觀念裡,文章是有等級的,亦即systematic review和meta-analysis的文章最有價值,single randomized controlled trial次之,其他類型的文章又次之,我們在搜尋文獻時也運用這個的觀念,先由重要的文章看起。
以下介紹幾個實證醫學網站
1. ACP’s PEIR: (ACP PIERc Physician’s Information and Education Reference w/ AHFS DIR Essentials) PIERc is a collection of over 400 evidence summaries published by the AmericanCollege of Physicians. Each module provides authoritative guidance to improve the quality of care.
Important features of PIER include:
Truly evidenced-based
Defines the current standard of care
Monthly updates
Structured for rapid access
Search or browse by organ system
Integrated drug reference
Website: http://www.statref.com/titles/details/PIER.html
2. UpToDate:
UpToDate is specifically designed to answer the clinical questions that arise in daily practice and to do so quickly and easily so that it can be used right at the point of care. The physician editors and authors review and update the content on a continuous basis and a new, peer-reviewed version is issued every four months. The published evidence is summarized and specific recommendations made for patient care. Website: http://www.uptodate.com/
3.Cochrane Library:
The Cochrane Library is a collection of databases that contain high-quality, independent evidence to inform healthcare decision-making. Cochrane reviews represent the highest level of evidence on which to base clinical treatment decisions. In addition to Cochrane reviews, The Cochrane Library provides other sources of reliable information, from other systematic review abstracts, technology assessments, economic evaluations and individual clinical trials – all the current evidence in one single environment.
Seven databases are included in Cochrane library:
| Database | Total Records |
| Cochrane Database of Systematic Reviews (CDSR; Cochrane Reviews) | 5171 |
| Database of Abstracts of Reviews of Effects (DARE; Other Reviews) | 7048 |
| Cochrane Central Register of Controlled Trials (CENTRAL; Clinical Trials) | 527,885 |
| Cochrane Methodology Register (CMR; Methods Studies) | 10,191 |
| Health Technology Assessment Database (HTA; Technology Assessments) | 7177 |
| NHS Economic Evaluation Database (NHSEED; Economic Evaluations) | <22,978 |
| About The Cochrane Collaboration (About; Cochrane Groups) | <92 |
Website:http://www3.interscience.wiley.com/cgi-bin/mrwhome/106568753/HOME
4. Pubmed Clinical Queries:
Pubmed Clinical Queries 是設在Pubmed資料庫下的一個搜尋引擎,主要是給臨床醫師使用,其內建的過濾器功能強大,主要分為clinical queries與systematic reviews兩大類別。使用者可以輸入關鍵字或問題,同時選擇查詢類別,系統會自動檢索,自PubMed 資料庫中篩選出有意義的檢索結果。在臨床查詢方面,有治療(therapy)、診斷(diagnosis)、病因(etiology)與預後(prognosis)四種功能可供選擇使用。而且可以使用敏感度(sensitivity)或特異度(specificity)兩種加強選項,讓搜尋關鍵字更具敏感性(sensitive)或特異性(specific)。另外,在systemic reviews方面,可以讓使用者搜尋系統審閱與整合分析(meta-analysis)的研究論述。
Website:http://www.ncbi.nlm.nih.gov/entrez/query/static/clinical.shtml
嚴格評讀文獻證據﹝Critical appraisal﹞
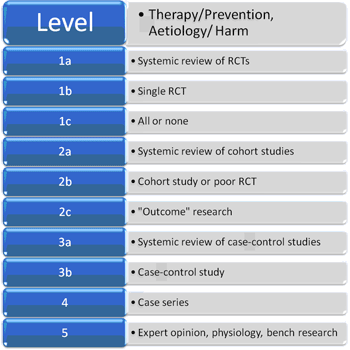 實證醫學臨床研究以統合分析(meta-analysis)、隨機對照臨床試驗(randomized controlled trials, RCT)、世代研究(cohort study)、個案對照研究(case control study)為主。雖然Cochrane強調使用RCT的重要性,然而實際上並無法於每一種醫療行為評估時找到相關且足以作為證據的RCT文獻。因此必須藉由其他方式的研究報告來做為證據來源,因此英國Oxford Centre定義了臨床研究的不同證據等級(Level of evidence)。有些議題因為醫學倫理的因素無法應用此種研究方法的時候,以實證醫學的方式,將相關此議題的文獻資料作統合分析後所獲得的結論更相形重要。
實證醫學臨床研究以統合分析(meta-analysis)、隨機對照臨床試驗(randomized controlled trials, RCT)、世代研究(cohort study)、個案對照研究(case control study)為主。雖然Cochrane強調使用RCT的重要性,然而實際上並無法於每一種醫療行為評估時找到相關且足以作為證據的RCT文獻。因此必須藉由其他方式的研究報告來做為證據來源,因此英國Oxford Centre定義了臨床研究的不同證據等級(Level of evidence)。有些議題因為醫學倫理的因素無法應用此種研究方法的時候,以實證醫學的方式,將相關此議題的文獻資料作統合分析後所獲得的結論更相形重要。
如何評讀一篇文獻資料,評估其可信度(Validity)、影響程度(Importance)及臨床可使用性(practicability),並作成結論是很重要的。要了解一篇研究的可信度應要知道其診斷試驗(diagnostic test)與疾病確立的參考標準(reference standard)是否互為獨立(independent)且試驗者與受試者互為雙盲(blind)?接受試驗樣本族群之選擇是否合適?以及疾病確立的參考診斷標準是否是否會依試驗結果來做決定?
而評核診斷試驗方法有效度常被使用的指標有: 1.敏感度(sensitivity,Sn)與特異度(specificity,Sp)。2.陽性預測值(positive predicative value, PPV)與陰性預測值(negative predicative value, NPV)。3.陽性相似比(positive likelihood ratio, LR+)與陰性相似比(negative likelihood ratio, LR-)。4.診斷試驗後疾病確定機率(post-test probability)
| Diseased | >Healthy | |
| Test result(+) | a (true positive) | b (false positive) |
| Test result(-) | c (false negative) | d (true negative) |
- Sensitivity (Sn) = 真陽性率 = 真陽性/生病者 = a/(a+c)
- Specificity (Sp) = 真陰性率 = 真陰性/健康者 = d/(b+d)
- Positive predicative value (PPV) =真陽性/陽性試驗結果 = a/(a+b)
- Negative predicative value (NPV) =真陰性/陰性試驗結果 = d/(c+d)
- Positive likelihood ratio (LR+) =真陽性率/假陽性率 =Sensitivity / (1-Specificity)
- Negative likelihood ratio (LR-) =假陰性率/真陰性率 =(1-Sensitivity) / Specificity
- 診斷試驗前的疾病可能性Pre-test probability = prevalence =(a+c)/(a+b+c+d)
- 診斷試驗前的疾病機會比率Pre-test odds = prevalence/(1-prevalence)
- 診斷試驗後的疾病機會比率Post-test odds = pre-test odds X LR
- 診斷試驗後的疾病可能性Post-test probability = post-test odds/(post-test odds +1)
| Likelihood ratio | 臨床意義 | |
| LR(+) | >10 | 高度排入疾病 |
| LR(+) | 5~10 | 中度排入疾病 |
| LR(+) | 2~5 | 低度排入疾病 |
| 1/2~2 | 不具臨床意義 | |
| LR(-) | 1/2~1/5 | 低度排除疾病 |
| LR(-) | 1/5~1/10 | 中度排除疾病 |
| LR(-) | <1/10 | 高度排除疾病 |
敏感度與特異度未必有臨床意義,而陽性與陰性預測值則會受盛行率所影響。相似比(likelihood ratio)則可應用於診斷試驗結果非二分法(即陽性與陰性)的試驗上。例如試驗結果為輕度、中度、重度之分,或是結果為連續數值,也就是說應用於多層級(multiple levels)的試驗結果上。
至於在評核治療效果時,則有一些數據是常被應用的。
- 對照組事件發生率 Control event rate (CER)。
- 實驗組事件發生率 Experimental event rate (EER)。
- 相對風險比率差 Relative risk reduction (RRR) = (CER-EER)/CER,為實驗組和對照組間產生的風險比率所降低的相對百分比。
- 絕對風險比率差 Absolute risk reduction (ARR) = (CER-EER),為實驗組和控制組產生不同結果比率之間的差異,此數據通常比相對風險比率差對治療效果評估較實用。
- 相對風險比率增加 Relative risk increase (RRI) = (EER-CER)/CER,為實驗組和對照組間產生的風險比率所增加的相對百分比。
- 絕對風險比率增加 Absolute risk increase (ARI) = (EER-CER)。
- 需要被治療的病人數目 Number needed to treat (NNT) =1/ARR ,絕對風險比率差異值的倒數,即使一位病人達到實驗組治療之有益結果(或預防產生一個不良結果)所需治療的病人數目。
- 需要被傷害的病人數目Number needed to harm (NNH) =1/ARI。除了考慮治療的好處外,也要考慮治療帶來的壞處,當病患接受了實驗組的治療後,可能會有病人產生副作用,亦即對多少病人數目進行實驗組療法,與對照組做比較後,會有多一個病人產生不良副作用。
評估一篇文獻的可信度和實用性,除應注意研究選入病人的條件,治療追蹤統計的方法,以及結果的定義,也應注意:病人樣本分組是隨機分配嗎? 分配方法是否遵守保密原則? 分配的不同組別在治療開始時的baseline是否相似?若不相似,是否用統計的方法來修正,或增加被研究者的數目,這些代表隨機分配的方法是否適當? 除了研究治療項目不同以外,其他變數在各組間是否相同? 治療方法對病患、醫護人員、研究者是否blinded(non-blinded, single blinded, double blinded, or triple blinded)? 追蹤是否完整? 分析時是否利用intention-to-treat analysis分析? 等等…都是考量一篇文獻其研究結果是否值得我們參考。
證據結論與臨床專業及病人價值結合及應用﹝Integrating the appraisal with clinical expertise and patients’preference﹞
當我們評讀完一篇文章且這篇文獻試驗的方法符合前述檢驗條件並被我們認為其數據結果是可信賴的,下一步即是如何將文獻中之方法實際應用於自己臨床醫療工作上了。這之間其實可能還有一段距離,包括自己的病人與文獻研究中之病人群體特性是否相近?病人對於我們告知的醫療知識理解有多少?實際醫院所能提供的資源有多少?病人配合的意願有多少?甚至是病人的經濟狀況或是後續照顧的配合等等..都會影響實際執行的成效。不過最重要的還是需與自己的專業和病人價值做結合才能達到最佳的應用。
評估執行效果及效用﹝Evaluation the effectiveness and efficiency in executing steps 1-4﹞
實際臨床應用執行之後,必須評估執行的程度及執行後的病人結果。並且回過頭來重新評估自己是否能再提出可回答的問題?是否能利用這樣的方法找到更多有用的文獻資料?是否能評讀文獻資料效度與臨床實用性?是否能結合評讀的證據於臨床應用上?這樣的方法有無改變自己診療照護的習慣?如自周而復始,以達到時時自我學習充實並不斷改進臨床治療,讓病人獲得最佳的治療效果。
實證醫學的重要性
處在目前這一個知識爆炸的時代,由於醫學知識大量且快速的累積,醫療的藥物,治療的方法,治療的儀器設備不斷的更新,許多臨床醫師在執行臨床醫療行為時,要做出有效、正確、且快速的抉擇更加不易。每年全世界約有6百萬篇的研究文獻發表於2萬種不同的生物醫學期刊上。然而更有專家指出,這些龐大的文獻資料中真正適合臨床工作者使用的大約只有百分之二十。對臨床工作者來說,要從浩瀚醫學文獻中將這百分之二十的醫學資訊找出、消化,並運用在每天的臨床作業中,在過去是一件相當費時且不容易的工作。所幸於1990代起伴隨著電腦科技的迅速發展,大量的文獻資料可載入電腦網路,網路醫療資訊的發展鼓舞了臨床醫療工作者,讓臨床醫療工作者可以從平面或電子管道迅速獲得大量文獻資料。據統計每月收錄至MEDLINE資料庫檢索系統的文獻約有33,000篇之多(Roche N., et al., 1994)。然而這些文獻的內容變異性很大,品質又很難評估下,於各別臨床工作者之間所產生的認知效果亦不同,臨床醫療工作者於資料判斷及應用上產生了很大的困難。新興網路醫療資訊與傳統統計學及流行病學的結合催生的實證醫學強調臨床問題分析、資料搜尋、嚴格評讀及應用的重要性,幫助臨床醫療工作者解決了這個困難。
另一方面,實證醫學的推動亦可幫助不同的醫療單位或個人對於疾病診療建立起適合自己條件環境的臨床作業指引。過去,對於病人的醫療照護決策,大多是靠著醫師本身的專業訓練與臨床經驗判斷來決定。通常醫師都以解決病人現有的問題或以他們過去的經驗來作出臨床決策與決定要如何使用醫療資源。但是研究發現,這些決策僅4%是有強而有力的臨床研究證據所支持,45%是有謹慎的臨床研究證據,且在醫師間有一定程度的共識,而剩餘51%的部份不但缺乏有力的證據支持,在醫師間亦無共識(Fieldm and Lohrm, Institute of Medicine, 1992)。而這些無共識的灰色地帶,往往造成醫師臨床操作上的差異性,造成不適當、過度醫療的產生,甚至許多醫療工作者過去的?經驗?經過學理的考證證明是錯誤的,而間接造成醫療資源的浪費與成本的增加。因此研發臨床作業指引的建立,則是提供臨床醫療工作者執行醫療工作時能有一個主要的參考依據,減少其診斷決策上的差異性與灰色地帶,而使所執行的每一項醫療行為更具科學證據的佐證,並提供病人更合適的照護。因此,臨床作業指引發展的主要目的包括(一)減少不必要的檢查、處置,並減少臨床操作的差異性。(二)增加病人照護的醫療效果,改善醫療品質。(三)降低或控制醫療照護成本。(四)改善臨床醫學教育訓練,推廣正確使用醫療科技與方法。(五)採用以證據為為主的診療行為,將醫學研究結果融入臨床診療作業中。目前台灣推行的健保制度,近來為控制醫療費用的龐大支出,推行醫院卓越計畫,給付制度改朝總額預算及自主管理政策執行,醫療單位若治療行為能依循臨床準則配合實證醫學精神,病人安全得到保障,醫療費用合理不浪費,可以達到雙贏局面。
實證醫學中心從1992年英國國家衛生服務院National Health Service Research and Development Program為紀念Archie Cochrane的貢獻,在牛津大學成立Cochrane Collaboration研究組織,希望與全世界專家針對各個醫學領域之隨機對照試驗作系統性評論,目前有英國、法國、美國、加拿大、澳洲、中國、巴西、荷蘭、義大利、西班牙、德國、挪威、南非等國家共15個Cochrane中心成立,並積極推動相關工作。希望能利用嚴謹且系統性的評估方法,從龐大的醫學研究資料庫中整理出截至目前為止各種醫療行為之結論性療效以改進醫療品質及資源運用。 Cochrane Collaboration 國際共同研究組織遵循Cochrane所提出對醫療行為之研究須合乎Randomized Controlled Trials的要求,系統性地隨時更新並發布醫療研究評讀的結果。


